こんにちは!ココモの唐沢です。
ダイビングで学科講習が必要な主な理由の一つ「減圧症のしくみ」について。
似たテーマには、ダルトンの法則や生理の減圧症、アドベンチャーのマルチプランがあります。
「ヘンリー((イギリスの化学物理学者。ウィリアムヘンリーはジョン・ダルトンとも知り合いだった。))の法則」を踏まえ、減圧症を防ぐ合理的な計画を立て、実施できる様になりましょう!
ヘンリーの法則とは
特定の温度で液体に溶け込む気体の量は、その気体の( )に正比例する。
《詳細》
気体の分圧《詳細を隠す》
「溶質((溶けつつある物質))」の分子が「溶媒((溶質が溶け込む物質))」の分子の中に均等に散らばり共存するが、それぞれは個々の振る舞いをする。
- 気体の溶解性に影響を及ぼす要素
- 圧力と温度。
- 溶解性(特定の液体と特定の気体の組み合あわせ。相性。)。
- (例)水には油より塩の方が溶けやすい
ダイビングでのポイント
ダルトンの法則と合わせて
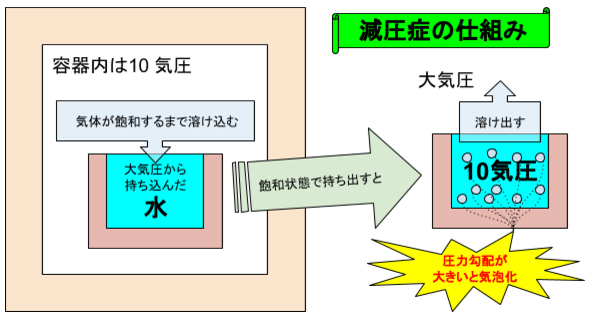
水と接しているそれぞれの気体は、水中の分圧がその気体の分圧と同じになるまで水に溶け込む。
-
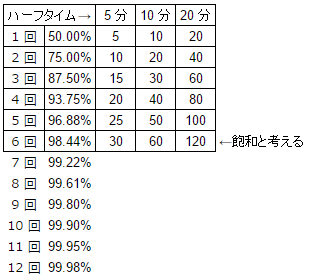
気体としての物質の分圧と、液体内に溶け込んだ物質の圧力の差は「( )」と呼び、溶け込むにつれこの差は小さくなり(勾配が低くなり)、気体が溶け込む速度が減少する。→ハーフタイム
《詳細》
圧力の差は「圧力勾配」と呼ぶ《詳細を隠す》
- 圧力勾配が0(ゼロ)になるとそれ以上の変化は起こらなくなり、気体が「( )状態」にあるという。
《詳細》
飽和状態《詳細を隠す》
- 実際は同数の液体から出たり入ったりが繰り返されている。
- ダイビングでの浮上、炭酸ジュースの開栓の様に、気体部分の圧力が減少すると、飽和状態から圧力勾配が逆転すると「( )状態」にあるという。
《詳細》
過飽和状態《詳細を隠す》
- 結果、水((溶媒))から溶け込んでいた気体((溶質))が溶け出す。
- 圧力勾配が非常に高い場合((拡散するより速いペースで気体が抜け出してくる場合))、気泡が形成される。
- 水((溶媒))を、激しくかき回すなどの要因がある場合、気泡が形成されやすくなる。
これが炭酸ジュースを例に挙げて解説される減圧症のしくみです。
練習問題を解いてみましょう
プロダイバーが携わる現場での潜水管理では外せない知識です。数値化して考えられるようになりましょう。
海で水をすくったコップを
圧力容器に入れ一週間にわたって容器に2.5気圧をかけ続け引き続き水面に置いていた。この液体中の気体の圧力は?
- 1 気圧
- 2.5 気圧
- 3.5 気圧
- この条件では答えが出せない
《詳細》
解答 b. 2.5気圧 液体中に溶け込む気体の圧力は平衡状態になり 2.5 気圧となる。
《詳細を隠す》
私たちの体の中のガス分圧は…
海抜数メートルで生活している場合近似値で・・・窒素分圧( A )、酸素分圧( B )
- 0.2 気圧
- 0.8 気圧
- 1.0 気圧
- この条件では答えが出せない
《詳細》
解答 合計は大気圧の1気圧として各分圧は次のとおり
- b 窒素分圧 = 0.8 気圧
- a 酸素分圧 = 0.2 気圧
《詳細を隠す》
ダイバーの体の状態は
 陸上で生活をしているときは( A )、深度下へ行くほど( B )へ向かい、限度を超えて浮上する状態では( C )になる。
陸上で生活をしているときは( A )、深度下へ行くほど( B )へ向かい、限度を超えて浮上する状態では( C )になる。
- 飽和状態
- 過飽和状態
- 平衡状態
- 減圧症
- 肺の過膨張生涯
《詳細》
解答 A. a=飽和状態、 B. c=平衡状態、 C. c=過飽和状態
補足)減圧症になるとは限らない
《詳細を隠す》
まとめ
 ダイビング活動と減圧症の関係はヘンリーの法則で説明できる。
ダイビング活動と減圧症の関係はヘンリーの法則で説明できる。
体の組織は肺を通して周囲の気圧にるガスの吸収と排出が行われ、移動すると深さ(圧力)ごとの平衡状態へ向かう。この際の圧力差を「圧力勾配」というが、特に浮上時、この圧力勾配が大き過ぎる(限界値((M値という)))を超える過飽和になる)と体内で窒素が気泡化する可能性が高くなる。
窒素の気泡が発生したからといって直ちに減圧症になるとは限らないが、逆に限界値を超えてなくても激しい運動など他の要因で気泡が増え、減圧症が発症する可能性がある。